»κΚœΙφΫΜΝςΈΔ–≈/Q»ΚΓΔΙψΗφ/“λ“ΒΚœΉςΓΔΆΕΗεΒ»Θ§«κΝΣœΒΙζΫΓ–Γ÷ζ ÷Θ®ΈΔ–≈Κ≈ΘΚsyt4000030818Θ©
±ΨΈΡΉς’ΏΘΚΙζΫΓ“Ϋ“©Ή…―·ΚœΙφ÷––ΡGSP ¬“Β≤ΩΉ …νΙΥΈ άΒά÷ΜΕ
11‘¬7»’Θ§ΙψΕΪFDAΖΔ≤ΦΓΕΙΊ”Ύ ≥ΤΖ“©ΤΖ…ζ≤ζΨ≠”ΣΤσ“Β¬δ Β÷ςΧε‘π»ΈΙήάμΑλΖ®Θ®’ς«σ“βΦϊΗεΘ©ΓΖΘ§≥θ≤Ϋ÷ΤΕ®ΝΥΙψΕΪ Γ––’ΰ«χ”ρΡΎ“―Ψ≠»ΓΒΟ ≥ΤΖΘ®Κ§ ≥”Ο≈©≤ζΤΖΘ©ΓΔ“©ΤΖΓΔ±ΘΫΓ ≥ΤΖΓΔΜ·Ή±ΤΖΓΔ“ΫΝΤΤς–Β…ζ≤ζΨ≠”Σ–μΩ…÷ΛΒΡ…ζ≤ζΨ≠”ΣΤσ“ΒΘ§ΦΑΗςΦΕ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈¬δ ΒΤσ“Β«ιΩω Β ©ΒΡΦύΕΫΦλ≤ιΚΆΉέΚœΙήάμΓΘ
Ρ«Ο¥Θ§’β“Μ–¬ΒΡ’ΰ≤ΏΘ§ΫΪΕ‘Έ“Ο«“Ϋ“©Ψ≠”ΣΤσ“Β”–ΡΡ–©”ΑœλΡΊΘΩ
1ΓΔ‘ωΦ”Τσ“ΒΉ‘≤ι¥Έ ΐ
Τσ“Β–η≥–ΒΘ÷ ΝΩΑ≤»Ϊ÷ςΧε‘π»ΈΘ§Ε®ΤΎΜρ‘Ύ“©Φύ≤ΩΟ≈ΦύΕΫΦλ≤ιΖΔœ÷Έ ΧβΘ§“‘ΦΑΤσ“ΒΖΔ…ζ ≥ΤΖ“©ΤΖΑ≤»Ϊ ¬Ι ΒΡ¥Π÷ΟΦΑ’ΌΜΊΒ»Β»«ιΩωΘ§’ΙΩΣΉ‘≤ιΓΘ
Ή‘≤ιΤσ“ΒΖ÷ΈΣ»ΐΖγœ’Β»ΦΕΘ§≤ΜΆ§Ζγœ’Β»ΦΕΤσ“ΒΟΩΡξΉ‘≤ι¥Έ ΐΗς≤ΜœύΆ§ΓΘ
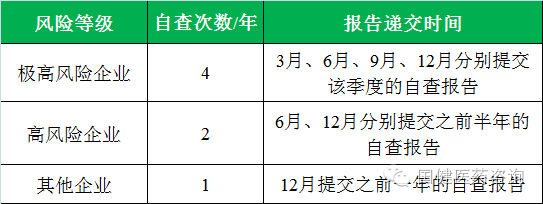
»γ”–Ψ≠”Σ¬ιΉμ“©ΤΖΓΔΨΪ…ώ“©ΤΖΓΔ“ΫΝΤ”ΟΕΨ–‘“©ΤΖΓΔΖ≈…δ–‘“©ΤΖΒ»ΧΊ βΙήάμ“©ΤΖΒΡΤσ“ΒΘ§”ΠΒ±Α¥’’ΦΪΗΏΖγœ’Τσ“Β“Σ«σΩΣ’ΙΉ‘≤ιΓΘ
2ΓΔ‘ωΦ”ΦύΙή≤ΩΟ≈Φλ≤ι¥Έ ΐ
–ΓΔœΊΦΕΦύΕΫΙήάμ≤ΩΟ≈ΜαΗυΨίΗςΒΊ ≥ΤΖ“©ΤΖΑ≤»Ϊ–Έ ΤΚΆΗςΦΕΦύΙήΉ ‘¥ΧθΦΰΘ§”ΎΟΩΡξΕΰ‘¬«ΑΑ¥’’ ≥ΤΖΓΔ“©ΤΖΓΔ±ΘΫΓ ≥ΤΖΓΔΜ·Ή±ΤΖΓΔ“ΫΝΤΤς–ΒΖ÷άύ÷ΤΕ®œ¬¥ο±ΨΡξΕ»ΦύΕΫΦλ≤ιΦΤΜ°Θ§Ος»ΖΦύΕΫΦλ≤ιΤσ“ΒΓΔΦλ≤ιΖΫΖ®ΓΔΦΤΜ°Φλ≤ι ±ΦδΒ»ΡΎ»ίΓΘ
ΦύΙή≤ΩΟ≈ Ι”Ο ιΟφΦλ≤ιΘ®Ή‘≤ι±®ΗφΜρœύΙΊΦΦ θΉ ΝœΘ©ΓΔ»’≥ΘΦύΕΫΦλ≤ιΓΔΖ…––Φλ≤ιΓΔΉ®œνΦλ≤ιΚΆΧεœΒΦλ≤ιΒ»Θ§ΉέΚœ‘Υ”ΟΓΘΗςΦΕ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈Α¥’’Ζγœ’Ζ÷ΦΕΚΆΆχΗώΜ·ΦύΙήΡΘ ΫΕ‘œΫ«χΡΎ≥÷–μΩ…÷ΛΒΡ…ζ≤ζΓΔΨ≠”ΣΤσ“ΒΩΣ’Ι»’≥ΘΦύΕΫΦλ≤ιΓΘΦύΙή≤ΩΟ≈ΗυΨί÷ΤΕ®ΒΡΦύΕΫΦλ≤ιΦΤΜ°Θ§ΩΣ’ΙΦύΕΫΦλ≤ιΙΛΉςΓΘ»γ”ωΒΫΧΊ β«ιΩω ±Θ§ΦύΙή≤ΩΟ≈Ω…“‘ Ε»Βς’ϊΦΤΜ°ΓΘ
¥Υ¥ΠΩ…Ω¥≥ωΦύΙή≤ΩΟ≈”–Εύ÷÷Φλ≤ι–Έ ΫΘ§»ΈΚΈ“Μ÷÷Φλ≤ιΙΐ≥Χ÷–ΖΔœ÷Έ ΧβΕΦΩ… ΙΦύΙή≤ΩΟ≈‘ωΦ”Φλ≤ι¥Έ ΐΓΘ
3ΓΔ÷ΒΒΟΉΔ“β
Τσ“Β‘ΎΉ‘≤ιΙΐ≥Χ÷–ΖΔœ÷”–¥φ‘Ύ ≥ΤΖΑ≤»Ϊ ¬Ι «±‘ΎΖγœ’ΒΡΓΔΜρœΫ«χ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈ΦύΕΫΦλ≤ι÷–≈–Ε®Φλ≤ιΫαΙϊΈΣ≤ΜΖϊΚœΒΡΘ§Τσ“Β”ΠΒ±ΝΔΦ¥ΆΘ÷ΙΨ≠”ΣΘ§≤ΔœόΤΎœρ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈ΧαΫΜΉ‘≤ι±®ΗφΘ§Ψ≠ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈ΚΥ ΒΆξ≥…’ϊΗΡΒΡΘ§ΖΫΩ…÷Ί–¬Ψ≠”ΣΓΘ
»γΙϊΤσ“ΒΆ§ ±”Β”– ≥ΤΖΓΔ“©ΤΖΓΔ±ΘΫΓ ≥ΤΖΓΔΜ·Ή±ΤΖΓΔ“ΫΝΤΤς–ΒΒΡΨ≠”ΣΖΕΈßΘ§‘ρ–ηΧαΫΜΥυΕ‘”ΠΨ≠”ΣΖΕΈßΒΡΓΕΤσ“Β¬δ Β÷ ΝΩΑ≤»Ϊ÷ςΧε‘π»Έ«ιΩωΉ‘≤ι±μΓΖΦΑΓΕΤσ“ΒΉ‘≤ι±®Ηφ’φ Β–‘≥–≈Β ιΓΖΓΘ
Ή‘≤ιΆξ≥…Κσ–κ”…Τσ“ΒΖ®Ε®¥ζ±μ»ΥΜρΗΚ‘π»ΥΕ‘ΓΕΤσ“Β¬δ Β÷ ΝΩΑ≤»Ϊ÷ςΧε‘π»Έ«ιΩωΉ‘≤ι±μΓΖΦΑΓΕΤσ“ΒΉ‘≤ι±®Ηφ’φ Β–‘≥–≈Β ιΓΖΫχ––«©ΟϊΦΑΧαΫΜΓΘ“‘÷Ϋ÷ ΜρΒγΉ”ΈΡΒΒΒΡ–Έ ΫΧαΫΜ÷Ν ≥ΤΖ“©ΤΖΦύΕΫΙήάμ≤ΩΟ≈ΓΘ
Ε‘’ς«σ“βΦϊΗε»‘”–“…Έ ΘΩ
≥ΛΑ¥ΕΰΈ§¬κΉ…―·Ή®Φ“

