2016ΡξΘ§Ε‘”Ύ“Ϋ“©Ψ≠”ΣΤσ“Βά¥ΥΒΘ§Έό“… «ΩΦ―ιΚΆΜζ”ωΥΪΫαΚœΒΡ“ΜΡξΓΘΒ±ΫώΖ…Φλ–¬≥ΘΧ§œ¬Θ§»ΪΙζΗςΒΊΖ…––Φλ≤ιœϊœΔ≥÷–χ≤ΜΕœΘ§Ζ…ΦλΉι±ι≤ΦΗςΒΊΘ§“©ΤσΩ…ΈΫΈ≈ΓΑΖ…ΦλΓ±…ΞΒ®Θ§“©Τσ≥Ζ÷ΛΜρœόΤΎ’ϊΗΡΙΪΗφ“ύ «ΓΑ±ιΒΊΩΣΜ®Γ±ΓΘ2016Ρξ5‘¬3»’ΙζΦ“ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΉήΨ÷ΖΔ≤ΦΓΕΙΊ”Ύ’ϊ÷Έ“©ΤΖΝςΆ®Νλ”ρΈΞΖ®Ψ≠”Σ––ΈΣΒΡΙΪΗφΓΖΘ®2016ΡξΒΎ94Κ≈Θ©Θ§“Σ«σΥυ”–»ΪΙζ“©ΤΖ≈ζΖΔΤσ“ΒΉ‘≤ι2013Ρξ7‘¬1»’÷ΝΫώ °œνΡΎ»ίΘ§≤Δ”Ύ2016Ρξ5‘¬31»’«Α±®ΥΆ Γ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΨ÷ΓΘΗυΨίΙζΦ“ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΉήΨ÷2016Ρξ6‘¬24»’Ά®ΗφΘ§Ης ΓΦΕ ≥ΤΖ“©ΤΖΦύΙή≤ΩΟ≈Έ¥ΧαΫΜ’ϊΗΡ±®ΗφΒΡ≈ζΖΔΤσ“Β ΐΝΩΈΣ370Φ“Θ§Ά®ΗφΫΪΗΟ–©≈ζΖΔΤσ“ΒΝ–ΈΣ÷ΊΒψΦλ≤ιΕ‘œσΘ§”…¥ΥΘ§»ΪΙζΖ…Φλ––Ε·Ηϋ «Ϋχ––»γΜπ»γί±ΓΘ
ΨίΥΒΘ§ΙψΕΪ Γ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΨ÷»ΐΗωΖ…––Φλ≤ι–ΓΉιΫϋΤΎ≥÷–χΕύΒΊΗΏΤΒ¬ ΫΜ≤φΖ…––Φλ≤ιΘ§ΥφΚσΙψΕΪ Γ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΨ÷Άχ’Ψ…œ≥Ζ÷ΛΜρœόΤΎ’ϊΗΡΙΪΗφΦΗΚθΟΩ÷ήΖΔ≤ΦΘ§± ’Ώ ’Φ·ΫΊ÷Ν2016Ρξ7‘¬31»’ΙψΕΪ Γ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΨ÷≥Ζ÷ΛΙΪΗφΚΆœόΤΎ’ϊΗΡΙΪΗφ ΐΨίΘ§Ά≥ΦΤ»γœ¬ΘΚ
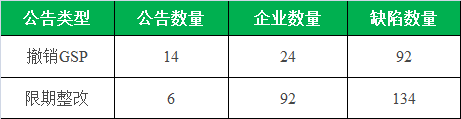
»±œίΗΏΤΒTOP10Ά≥ΦΤ»γœ¬ΘΚ
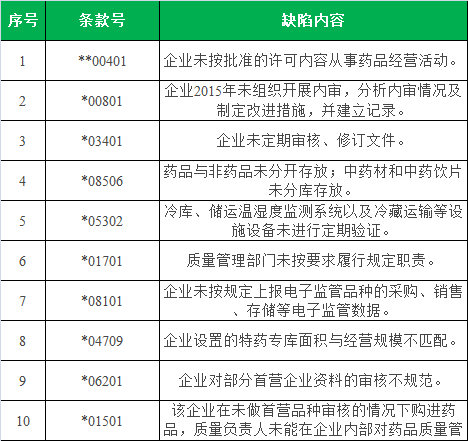
2016Ρξ7‘¬20»’Θ§ΙζΦ“ ≥ΤΖ“©ΤΖΦύΕΫΙήάμΉήΨ÷ΖΔ≤Φ–¬–όΕ©GSPΘ§Βς’ϊ≤ΩΖ÷ΡΎ»ίΘ§Ε‘”Π“‘…œ± ’ΏΆ≥ΦΤ≥ωΒΡ»±œίTOP10Θ§“©Τσ–ηΧΊ±πΝτ“β“‘œ¬»ΐΒψΘΚ
1ΓΔΒΎ»ΐœνΘ®*03401Θ©–ηΗυΨί–¬ΑφGSP…ξ«κΤπ≤ί–όΕ©ΧεœΒΈΡΦΰΘ§ΦΑ ±Βς’ϊ–¬ΡΎ»ίΘΜ
2ΓΔΒΎΤΏœνΘ®*08101Θ©–¬ΑφGSP»ΓœϊΒγΉ”ΦύΙή÷ΤΕ»ΚΆœύΙΊΙφΕ®Θ§Ε‘”ΎΙψΕΪ ΓΗω–‘Μ·“Σ«σΘ§–ηΦΑ ±≤…ΙΚΓΔœζ έΓΔΩβ¥φΒ»“ΒΈώ ΐΨί…œ¥Ϊ÷ΝΙψΕΪ ΓΤσ“ΒΟ≈ΜßΤΫΧ®ΘΜ
3ΓΔΒΎΨ≈œνΘ®*06201Θ©–¬ΑφGSPΡΎ»ίΒς’ϊ÷°“ΜΘ§ΗϋΗΡ Ή”ΣΤσ“ΒΉ Νœ ’Φ·“Σ«σΘ§¥”2016Ρξ7‘¬20»’Θ§ Ή”ΣΤσ“Β–η―œΗώΑ¥’’Ήν–¬“Σ«σ ’Φ· Ή”ΣΉ ΝœΘ§¥ΥΚσ±Θ≥÷“ΒΈώΆυά¥ΒΡΙ©ΜθΒΞΈΜΘ§Ϋ®“ι“≤ΨΓΩλΑ¥’’Ήν–¬“Σ«σ ’Φ·Τσ“ΒΉ ÷ Ή Νœ¥φΒΒΓΘ
“‘…œΫωΈΣ± ’ΏΗω»ΥΆ≥ΦΤΚΆΦϊΫβΘ§± ’Ώ»œΈΣΘ§‘Ύœ÷Ϋώ–Έ Τ÷–Θ§“©Τσ–ηΦΑ ±≤ΕΉΫΚΆœλ”ΠΙζΦ“ΚΆΒ±ΒΊ’ΰ≤ΏΘ§Ω…Ρή«ΑΤΎΜα”ΑœλΤσ“Βάϊ»σΘ§ΒΪΆυΆυΓΑ Θ’ΏΈΣΆθΓ±Θ§“©Τσ–ηΥΦΩΦ»γΚΈΈ»ΙΧ –≥ΓΓΔΚœΙφΨ≠”ΣΘ§¥”ΕχΦΧ–χ±Θ≥÷‘Ύ“©ΤΖΝςΆ®Νλ”ρΒΡ…ζ¥φΓΘ
